吴庆华医生的科普号
- 精选 网上预约门诊途径已更改!
因北部院区和总院系统完全合并,网上预约已改至公众号:上海交通大学医学院附属瑞金医院,敬请关注!
 吴庆华 副主任医师 上海瑞金医院 普外科2031人已读
吴庆华 副主任医师 上海瑞金医院 普外科2031人已读 - 精选 甲状腺结节问答——大家可以了解一下
这是我受邀做“健康有道”访谈节目,做关于甲状腺结节的一些常见问题的答疑,大家可以了解一下!(下面是两个链接)
 吴庆华 副主任医师 上海瑞金医院 普外科3885人已读
吴庆华 副主任医师 上海瑞金医院 普外科3885人已读 - 诊前须知 复工开诊通知:
【通知】7月1日始北部院区正式复工开诊,门诊按原来排班,个人还是周一上午周六上午专家门诊,周二上午特需门诊。特此告知!
吴庆华 副主任医师 上海瑞金医院 普外科247人已读 - 媒体报道 突发的紧急保障任务,脱产一月
因众所周知原因,身为支部书记带队保障,义不容辞,脱产一月余。请各位见谅,当然有事还是可以随时平台联系的!
 吴庆华 副主任医师 上海瑞金医院 普外科2128人已读
吴庆华 副主任医师 上海瑞金医院 普外科2128人已读 - 诊后必读 关于甲状腺术后打疫苗的问题的统一回复!!
很多甲状腺术后的病人对于近期打疫苗的事颇有疑虑,在此统一回复:除去特殊过敏体质等不论,甲状腺术后在甲状腺功能(FT4,TSH)尚未平稳、比较疲劳(免疫力低下)阶段(一般三月内),不建议接种疫苗外,都可以接种;当然,也需要注意接种后可能有的反应。
 吴庆华 副主任医师 上海瑞金医院 普外科5508人已读
吴庆华 副主任医师 上海瑞金医院 普外科5508人已读 - 学术前沿 生物补片成为青少年腹股沟疝修补材料中比较理想的选择——专家共识
孙 立,陈 杰. 青少年腹股沟疝治疗中应用补片的争议、共识及合理选择[J]. 中国实用外科杂志,2019,39(8):798-800.
 吴庆华 副主任医师 上海瑞金医院 普外科2173人已读
吴庆华 副主任医师 上海瑞金医院 普外科2173人已读 - 论文精选 转:美国甲状腺协会关于颈外入路甲状腺手术的声明解读
结论第1条-颈外入路ETS在特定情况下具有重要临床意义,鼓舞人心!原创 中国实用外科杂志2017,37(9) 摘要 内镜下甲状腺切除术(endoscopic thyroid surgery, ETS)的发展已历经20年。随着器械与设备的更新,尤其是高清内镜与机器人辅助系统的应用,如今已经在世界范围内逐渐推广,并不断发展创新。美国甲状腺协会(ATA)于2016年发表了颈外入路内镜甲状腺手术声明。通过系统性回顾文献及综述,对颈外入路ETS的发展历程进行了归纳,以推动ETS规范、安全、有序地开展,并指导临床。该声明对于手术方式、治疗结局、术后并发症、发展障碍等方面进行了全面、系统的阐述。 2016年,美国甲状腺协会 (American Thyroid Association,ATA) 发表了关于颈外入路内镜甲状腺手术的声明[1]。内镜甲状腺手术(endoscopic thyroid surgery,ETS)在美国发展较缓慢,因而该声明主要通过回顾大量文献,对颈外入路ETS的开展提出专家意见。笔者拟对该声明进行解读,以期帮助国内同行了解国际现状、规范临床实践。ETS根据入路不同分为颈前入路(近距离入路)、颈外入路(远距离入路)及经自然腔道入路(如经口腔内镜下甲状腺切除术)。该声明主要阐述颈外入路ETS。这也是ATA关于内镜甲状腺手术的首次官方发声,由ATA外科部远距离手术委员会负责,工作组主要由头颈外科和内分泌外科医生组成。 1.常用的4种颈外入路ETS 1.1 经胸前入路ETS 由Ohgami等[2]于2000年报道,其手术切口在双侧乳晕,经胸前皮下和颈阔肌平面下行皮瓣游离,建立人工腔道,持续充入CO2并维持压力在5~6 mmHg (1 mmHg=0.133 kPa),应用内镜器械完成甲状腺切除术。共对5例病人行甲状腺切除术,肿瘤直径在5~7 cm,术后均无并发症发生。 1.2 经双侧腋乳入路内镜或机器人ETS Shimazu等[3]报告了单侧腋窝-乳晕入路(axillo-bilateral-breast approach,ABBA)手术。2007年,Choe等[4]在其基础上进行了改良,开展了双侧腋乳入路(bilateral axillo breast approach,BABA入路),即双侧腋窝双侧乳晕入路。其在双侧乳晕建立12 mm通道,分别放置镜头和超声刀,双侧腋窝建立5 mm通道用于放置抓钳和分离钳(图1),CO2充气法维持手术空间。该方法对双侧腺体的暴露较好,其甲状腺切除步骤与开放手术类似,但该方法对内镜外科技术要求较高,难以掌握。故Lee等[5]于2009年将机器人辅助系统用于BABA入路甲状腺切除术。因机器人辅助系统具有更好的内镜放大效果和可360?旋转的EndoWrist操作臂,学习曲线缩短。 1.3 经腋窝入路内镜或机器人ETS 腋窝入路最初由Ikeda等[6]开展,系在腋窝处行一3 cm切口,置入12 mm和5 mm trocar。随后充入4 mmHg CO2气体,在其附近再置入另一5 mm trocar。分离胸锁乳突肌和甲状舌骨肌,进入颈部正中,进行甲状腺切除。Yoon等[7]于2006年对该法进行了改进,其采用免充气悬吊法,采用腋窝一5~6 cm切口,游离皮瓣至锁骨。放置固定牵开器上提皮瓣,然后连接机器人辅助系统(图2),通过腋窝单孔置入3或4个机械臂。该方法的优点是免充气,不足在于腋窝皮瓣的建立需要较长学习曲线,另外通过单个切口切除对侧甲状腺比较困难。因而有学者建议对于甲状腺全切除病人行双侧腋窝切口。但也有学者认为使用30?镜并将床转向镜头,即可充分暴露对侧腺体[8]。由于手臂伸展可能会造成臂神经的损伤,目前临床已出现更为保守的体位,即同侧肢体肘关节和肩关节的微伸展体位。 1.4 经耳后入路内镜或机器人ETS Terris等[9]开展了耳后入路,结合免充气技术与耳后切口完成甲状腺切除术(图3)。该技术在耳后皮纹或附近做切口,在耳廓可遮蔽位置延伸至枕骨发际线。使用固定拉钩牵拉皮瓣。该方法的优点是在所有颈外入路中此入路路径最短、创伤最小且免CO2充气,也不受病人体重指数(BMI)及肿瘤最大径的限制,尤其适合欧美病人。但该入路解剖视角为自上而下,且对侧腺体操作受限。 颈外入路甲状腺手术仅改变了手术入路,其治疗原则应与开放手术相同,病人的治疗应基于ATA关于甲状腺结节的处理指南[10]。甲状腺切除术的适应证应与开放手术相同,病人的选择应综合评估病人及疾病因素,并根据各入路的特点选择合适的手术方式。 2.治疗效果及并发症 多数颈外入路甲状腺切除术的报道来自韩国。目前样本量最大的是Ban等[11]报道的3000例经腋窝机器人甲状腺癌手术。该队列主要是体型较瘦病人(BMI为22)组成,且多为小结节(平均直径0.66 cm):80%为甲状腺微小癌;19%为非微小癌,肿瘤最大径为6 cm。甲状腺全切除术的手术时间为141 min,非全切除术在115 min内。并发症发生情况与常规甲状腺切除术类似,包括暂时性症状性低钙血症(37.0%)、永久性低钙血症(1.0%)、暂时性喉返神经损伤(1.2%)、永久性喉返神经损伤(0.3%)、皮下积液(1.7%)和血肿(0.40%),以及其他一些较罕见并发症如乳糜漏(0.4%)、气管损伤(0.20%)、Horner综合征(0.03%)、颈总动脉损伤(0.03%)、无名静脉损伤(0.03%)等。另外该技术可引发新的并发症如牵拉伤(0.1%)和腋窝皮瓣穿孔(0.1%)。Lee等[12]也报告了1026例BABA机器人手术,病人具有与上述队列相似的特征:平均年龄40岁,甲状腺结节直径平均0.8 cm,其中81%为微小癌。 韩国的数据表明,接受ETS者多为早期病例,术者手术量巨大,积累了丰富经验,但声明认为正是基于早期病例,即便经验非常丰富的医生仍有可能出现各种并发症,建议这些手术在特定的中心由经验丰富的手术团队按照严格的程序进行。 尽管机器人甲状腺切除术在韩国已普及,但由于病人人群、医疗模式和病人关注点的差异,美国的接受速度较慢。美国病人BMI较大且结节较大。Kuppersmith等[13]对31例病人开展了经腋窝入路机器人甲状腺切除术,该报道强调了这些差异:病人平均BMI为25(18~34),结节直径为2.7(1.0~4.6)cm。66.7%的病人为腺叶切除,其余均为甲状腺全切除。术中数据同时突出显示了该技术的学习曲线,第一队列甲状腺全切除总手术时间平均为278 min,第二队列为168 min。 1例病人发生神经失用症,1例发生暂时性声带麻痹,2例病人因颈前静脉损伤发生术中出血(出血量>500 mL)。 Kandil等[14]报告了迄今为止美国最大样本的经腋窝机器人甲状腺切除术,共91例病人、100例次手术。病人平均BMI为28.5(16.0~55.0),结节直径平均为2.4 cm。70%病人行单侧甲状腺切除,并发症发生率为20%,包括皮下积液(4%)、切口感染(1%)、气管损伤(1%)、暂时性声音嘶哑(7%)、暂时性低钙血症(10%)、神经失用症(1%)。腺叶切除的手术时间为108 min,甲状腺全切手术时间为118 min。在同一研究中,肥胖病人(BMI>30)总手术时间显著增加(37 min)。尽管正常体重和超重病人的并发症相似,但肥胖病人预期面临更大的技术挑战。 在美国,经耳后机器人甲状腺切除术的经验更为有限。样本量最大的研究为Terris等[15]报告的14例病人的18例次手术。病人平均BMI为27,手术时间为155 min;除第1例外,均在门诊完成,且未放置引流。有2例发生皮下积液,1例发生暂时性声带功能障碍。Kandil等[16]随后报告了12例耳后入路机器人单侧甲状腺切除术,手术时间为156 min,其中9例(75%)发生轻度并发症,包括2例皮下积液、3例感觉异常、3例暂时性低钙血症和1例暂时性声音嘶哑。 最近一项回顾性研究报道了美国2010—2011年接受甲状腺切除术的6万例甲状腺癌病人[17],其中225例为机器人手术。与开放手术组相比,机器人手术组病人较年轻(51岁 vs. 47岁),且多为亚洲和私人投保病人。女性或腺叶切除病人更倾向于选择机器人手术。在多变量分析中,两组病人清扫的淋巴结数量差异无统计学意义。 与韩国相关报道相比,来自美国的少量经验更加强调疾病的特点的和病人特征。声明认为,由于目前数据有限,须特别注意新技术以及因手术时间延长可能带来的罕见并发症,特别是应考虑到这些病人与大多数开放手术病人相比病情更为简单。 3.术后并发症、美容效果及生活质量与传统甲状腺切除术的比较 在术后并发症方面,最近1项包含2375例病人的Meta分析显示,机器人手术与传统开放甲状腺切除术相比,前者手术时间(平均相差56 min)、住院时间更长,暂时性喉返神经损伤发生率较高,而在术中出血、低钙血症和总的并发症发生率方面两组差异无统计学意义[18]。 在美容效果满意度方面,文献[19-20]均认为ETS组术后早期美容效果满意度更高。文献[19]的研究中,机器人手术组病人对美容效果均满意,而开放手术组有8例(18.6%)病人表示不满意,1例(2.3%)非常不满意。但也有评论认为,开放手术病人瘢痕及色素沉着有望在术后1年减退,届时其美容满意度评分可能增加。 在术后生活质量方面的评估方面,多项研究采用术前、术后病人的自我评估,以及由专业人员进行的客观评估,结果显示ETS对术后病人的语音及吞咽功能的影响与开放手术相比差异无统计学意义[19,21-22]。 最近一项关于手术安全和肿瘤治疗彻底性的Meta分析显示,与常规甲状腺切除术相比,机器人手术失血量更少、美容满意度更高、吞咽损伤程度更轻;但前者手术时间更短,甲状腺癌病人清除的淋巴结更多[23]。 以上数据表明,颈外入路甲状腺手术与开放手术相比,在并发症总发生率方面差异无统计学意义,对发音及吞咽的影响与开放手术相比差异亦无统计学意义,而术后短期美容效果满意度较高。但在肿瘤治疗等效性上,尚缺乏随机临床试验或具有长期随访数据的对比研究。 4.学习曲线 与传统内镜ETS相比,有报道机器人手术技术学习曲线更短,但两种技术的手术时间均随经验的积累而缩短,分别于35~40例机器人手术以及55~60例内镜手术后趋于稳定[24]。一项前瞻性多中心研究发现,经验较少的外科医生平均手术时间较长、并发症发生率较高[25]。然而,一旦这些医生施行了50例机器人甲状腺全切除或40例次全切除术后,其手术时间和并发症发生率则与经验丰富的外科医生类似。来自美国的经验也建议至少行40例颈外入路ETS以完成该学习曲线。一项大样本研究显示,45例机器人手术后,总的手术时间可从122 min降至104 min(P=0.02)[14]。 5.费用及其他问题 Cabot等[26]的研究比较了颈部开放手术、经腋窝ETS和经腋窝机器人ETS在美国的手术费用,结果显示颈部开放手术费用显著低于经腋窝ETS,而后者又显著低于经腋窝机器人ETS。而当手术时间缩短时,费用的差异逐渐减少;当机器人和内镜手术的总手术时间分别减少至68 min和111 min时,则3种手术的成本相当。目前,大多数关于机器人ETS的研究来自于韩国,该国机器人甲状腺手术的报销额度为开放甲状腺手术的5倍。机器人手术的高成本来自于相关机器使用、较长的手术时间以及相关设施和人员费用。与传统甲状腺切除术相比,因手术时间更长,颈外入路技术并不具有成本效益,而机器人手术因额外的器械和材料可能造成更高的成本花费。 尽管ETS对技术要求更高、手术游离范围更广,但是对于少部分病人来说,由于美容需求或瘢痕增生病史,避免颈部切口有重要意义。颈外入路技术的运用和可行性使这些病人的愿望得到尊重和实现。 对于颈外入路ETS的认证目前尚无统一的规则,声明建议从最简单的腺叶切除开始,具备一定经验后再开展更为复杂的手术。 6.结论及建议 因病人选择、技术难度、费用和医疗制度等原因,目前开展颈外入路ETS尚存在一些障碍。但数据显示,颈外入路ETS已可在部分大中心安全开展。基于此,该声明特提出以下建议:(1)颈外入路ETS在特定情况下具有重要临床意义。(2)应严格遵守操作规范以确保手术安全。(3)由于该手术需要更高的技术水平,应由经验丰富的甲状腺外科医生经过正规培训后开展。(4)建议继续评估颈外入路ETS的治疗结局,以进一步修订其适应证。 此次ATA声明从手术方式、治疗结局、术后并发症、学习曲线、手术费用等方面对ETS进行了全面、系统的阐述。我国对于ETS也已有大量自己的经验积累[27-30],总体治疗原则与ATA类似,只是在医疗制度及医保政策方面各国规定不同。
吴庆华 副主任医师 上海瑞金医院 普外科2398人已读 - 媒体报道 2016世界内镜外科大会
 吴庆华 副主任医师 上海瑞金医院 普外科1582人已读
吴庆华 副主任医师 上海瑞金医院 普外科1582人已读 - 医学科普 沪上首例3D腔镜全乳晕甲状腺切除术报道
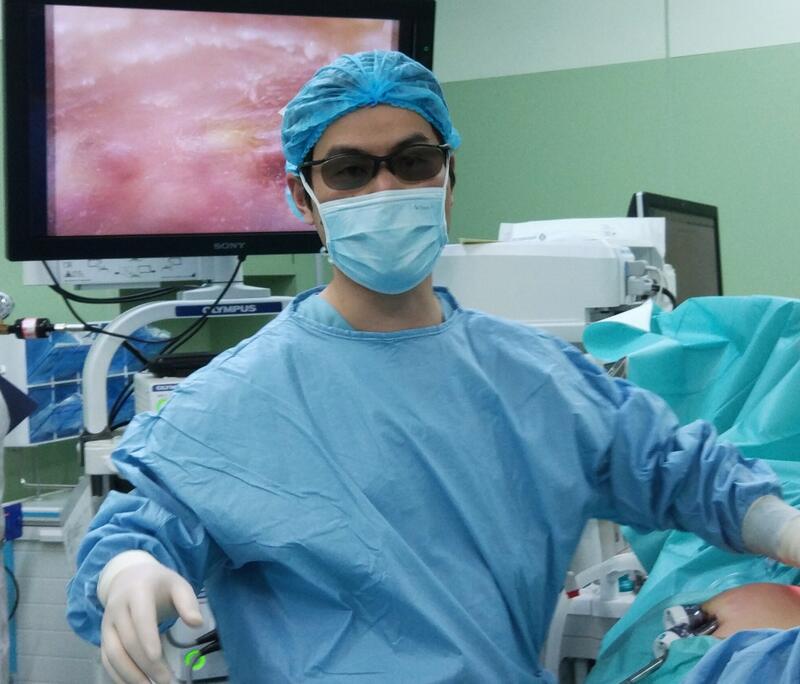
“身临其境、纤毫毕现”的3D立体腔镜颈部无瘢痕甲状腺手术 3D电影因为画面立体感强、富于冲击力,能够带给观众更加身临其境的感觉,我们团队在大量腔镜技术经验的积累下,进一步将3D影像技术应用于颈部无瘢痕全腔镜甲状腺手术中,开展了上海首例3D立体腔镜微创颈部无瘢痕甲状切除手术。传统的2D腔镜中所有组织显示在一个平面上,缺乏开放性手术的景深感觉,术中操作时难以感知解剖深度,增加了手术操作的难度。随着科技的发展,3D成像技术逐渐应用于医学领域,1992年Becker使用第一代3D立体视频显像技术进行了胆囊切除术,手术效果优于传统腹腔镜,但是第一代的3D立体腔镜系统存在着许多缺陷,如光源昏暗、术野显示模糊等,而且采用头戴式显示器,体积庞大、佩戴笨重。受限于当时技术,3D立体腔镜并未得到推广。偏光式3D立体显示技术以及高清3D显示屏的出现,可以呈现高分辨率的立体影像,很好地解决了第一代3D腔镜所存在的问题,尤其 “景深”感觉的出现,能够恢复外科医生对解剖深度的感知,能够使解剖层次更加精确、肿瘤边界更加确切、操作更加精准。经过偏光式3D腔镜的立体放大后,动脉、静脉、神经和肌肉层次都清晰可见,给术者“身临其境”的感觉。生理条件下,立体视觉的实现源于双眼视差,双眼均向同一物体聚焦成像,大脑将双眼图像差异部分滤过并将相似部分匹对后产生视差信息,最后通过中枢神经处理视差信息,左右眼图像融合形成一张立体图像,在大脑内形成深度感。3D腔镜立体成像原理则是模拟人双眼视差的原理,用3D双通道高清摄像头采集左右图像,由2条数字光学通路传送到一个3D数字处理单元进行分配,并最终传输到高分辨率显示器上,术者及助手通过佩戴轻重量的3D偏光式眼镜进行图像过滤,获得具有立体感、层次感、放大4~5倍的3D立体图像。2016年3月7日,邱伟华主任医师和吴庆华副主任医师在瑞金医院北院完成了上海市首例3D立体腔镜微创颈部无瘢痕甲状腺切除手术。患者李*良,男性,40岁,体检发现甲状腺结节,超声见:左甲状腺中上部近外侧21*9.2*13毫米肿块。虽然患者肿瘤>1厘米,但是根据患者的年龄、病情、体型和美容需求,和患者充分沟通后决定进行3D立体腔镜微创颈部无瘢痕甲状腺切除术。借助于术中偏光式3D立体腔镜镜头以及高清3D显示屏,“纤毫毕现”地呈现出颈部动脉、静脉、神经甚至毛细血管完美的立体影像,相比2D腔镜手术,3D腔镜手术仅耗时1.5小时,出血量仅10毫升,更加精准地切除了肿瘤。患者术后10天随访,恢复非常快速,没有任何不适。3D腔镜相对传统腔镜手术具有更多优点:(1)手术视野呈现立体感及层次感的。传统腹腔镜的二维成像缺乏纵深感是其最大的缺陷,而3D腔镜提供了一个近似直视下的三维立体图像,使术者操作更加精确,手术操作一步到位,同时可减少术中出血量及周围神经、组织的误伤。(2)提高手术性能。3D腔镜相比于2D腔镜,其擦镜头的次数明显减少,且在接近于真实的解剖视野下,使操作时间减少,也使手术安全性得到了提高。(3)增加操作环境舒适度。3D腔镜的立体视野弥补了传统2D腔镜呈现在术者面前单眼视觉图像的缺陷,从而可提供舒适的操作环境。(4)3D腔镜手术既能明显减少患者的手术创面,又能让术者获得多方位、多角度的视野,定位准确、空间分辨高等均反馈给术者良好的视觉和操作体验。当然3D腔镜也存在局限性,3D成像系统是2个双路平行摄像系统组成的三维立体腔镜,其镜身在Trocar中的旋转角度没有2D腔镜大,而且其调整视野时相对较困难。此外,2D腔镜是30度侧视镜头,而3D腔镜是0度正视镜,因此从更多轴心角度进行多方位观察,才能获得更加全面获得局部解剖结构信息。 甲状腺疾病发病率逐年升高,外科手术是其主要治疗方式之一。100余年前Kocher开创的颈前领式切口手术仍是目前临床应用最广泛的术式,但该术式会在颈部遗留长短不一的瘢痕,影响外观,爱美或需保守疾病隐私的患者难以接受。近年随着腔镜外科的发展,以及患者对于美观的需求,使得腔镜在甲状腺手术中也得到了很好的应用。3D腔镜已成熟应用于临床 ,但其应用在甲状腺手术的报道尚不多见。由于颈部位于人体“咽喉要道”,众多血管、神经、淋巴管密如“蛛网”,由于颈部缺乏自然腔隙,要在狭小的空间下完成手术,又要保护好喉返神经、喉上神经、甲状旁腺等重要结构,术者需要具备非常丰富的临床经验和扎实的手术功底。3D立体腔镜甲状腺手术时解剖层次更清楚、立体感更强、操作更精准、视觉放大效应更加显著,术中更容易准确识别、定位并避开和保护重要解剖结构如喉返神经和甲状旁腺。3D立体腔镜甲状腺手术的众多优点,相信会成为患者不错的选择,也会使传统外科向微创外科的发展再往前迈进一步。
吴庆华 副主任医师 上海瑞金医院 普外科2502人已读 - 学术前沿 NCCN 直肠癌指南(2015最新版)更新要点
NCCN 直肠癌指南(2015.2 最新版)一.重要的更新内容:1.FOLFOX、CapeOX 作为优选方案用于 pT3-4,N0 或 pT1-4,N1-2。2.围手术期化疗不超过 6 个月。3.手术切除前加入了如下治疗选择:先化疗(FOLFOX [优选]、CapeOX [优选]、5-FU/LV 、卡培他滨),然后再化放疗(卡培他滨 +RT [优选]、)输注 5-FU+RT [优选、静脉 5-FU/LV+RT]。4.FOLFOX+Cetuximab 作为治疗选择时需注意如下注释:对潜在可切除肝转移疾病的治疗数据仍有争议。5.检测 RAS 基因状态,包括 KRAS 外显子 2 和非外显子 2 以及 NRAS,还需检测 BRAF 基因状态。6.对术前化疗有反应的病人可能无法获得 12 个淋巴结。二.概述结直肠癌发病率和死亡率一直位于前列,随着预防策略、早期诊断和更佳治疗模式发展其发病率和死亡率呈下降趋势,但数据显示小于 50 岁年轻患者发病率上升,到 2030 年 20-34 岁人群直肠癌发病率可能增加 124.2%,原因不清。直肠癌 NCCN 指南与结肠癌指南有重叠之处,尤其是转移性疾病治疗。三.风险评估参见 NCCN 结肠癌指南(2015.2 最新版)四.分期第七版 AJCC 分期手册对直肠癌分期作了部分调整。T4 细分为 T4a 和 T4b。N1 和 N2 也进一步细分,反应受累淋巴结数量对预后的影响。浆膜下层、肠系膜、非腹膜的结肠周围或直肠周围组织肿瘤沉积定义为 N1c,反应了区域淋巴引流区肿瘤沉积对预后的影响。五.病理病理分期主要通过手术标本检查划分。一些需要详细记录的信息包括:肿瘤和标本大体描述,癌症分级,穿透深度以及向周围结构延伸程度,肿瘤区域淋巴结评估,阳性区域淋巴结数量,远处转移或非区域淋巴结受累,近端、远端和环周切缘,新辅助治疗效果,淋巴血管侵袭,神经周围侵袭,肿瘤沉积数量。1.边缘第七版 AJCC 分期手册包括如下建议:外科医生应标记标本中肿瘤侵袭最深区域以便病理医生直接评估切缘状态;切除的完整性包括 R0 切除,指肿瘤完全切除且边缘阴性,R1 不完全肿瘤切除,存在镜下边缘受累,R2 切除是不完全切除,有肉眼可见残存肿瘤。环周切缘(CRM)是直肠癌中重要的病理分期参数,对完全由浆膜包绕的结肠,根治性切缘指的是腹膜缘,CRM 对没有完全包绕或仅部分包绕的结肠或直肠非常重要。CRM 是肿瘤浸润最深处与肿瘤最近的直肠外软组织(例如肿瘤的后腹膜面或下腹膜面)间的部分,或是从淋巴结边缘计算,以 mm 计量,CRM 的确定要通过评估直肠和直肠系膜外缘标本,后者常需以墨水标记最外表层和面包片样的切片标本。委员会认为 CRM 距横切缘小于 1mm 为阳性。已切除直肠肿瘤标本的 CRM 病理学评估的重要性在于 CRM 是局部复发和总生存的强预测因子,包括新辅助治疗病人,而且是决定术后治疗的一个重要考量因素。如果只是淋巴结内肿瘤 CRM 阳性,应记录,因为有研究显示淋巴结内 CRM 阳性同肿瘤直接延伸的 CRM 阳性相比复发率较低。2.淋巴结AJCC 和 CAP 推荐评估 10-14 或 12-18 个淋巴结以准确评估早期结直肠癌。能检测的淋巴结数量与病人年龄、性别有关,也与肿瘤分级和位置有关。新辅助治疗后获取淋巴结数目可能减少,可以作为治疗有效反应指标。目前有关微转移或前哨淋巴结检测癌细胞的研究仍有争议,不将其用于做出临床决定。3.治疗反应AJCC 手册和 CAP 指南要求病理报告要对新辅助治疗效果进行评价,至少要评价是否为根治性治疗效果。更优化的评价是对肿瘤反应采用评级:0-3 级,0 为完全反应,没有活细胞可见;3 为反应差,很少或没有肿瘤细胞杀伤,大量肿瘤细胞残留。4.神经周围侵袭神经周围侵袭与预后差相关。5.淋巴结外肿瘤沉积结外肿瘤沉积或卫星结节是不规律分散的肿瘤沉积于直肠周围脂肪中,与肿瘤边缘不连续,也非淋巴结残留,但位于原发肿瘤的淋巴引流区域内,并不计入淋巴结。大多数肿瘤沉积认为是淋巴血管侵袭或神经周围侵袭。结外肿瘤沉积数量也应计入病理报告,与 DFS 和 OS 降低有关。结外肿瘤沉积分作 pN1c。六.维生素 D 在结直肠癌中的作用参见 NCCN 结肠癌指南(2015.2 最新版)七.非转移性疾病的临床表现和治疗1.治疗息肉样癌对内镜切除腺瘤样息肉或绒毛样腺瘤做出手术切除决定前,医生应回顾病理并与病人沟通。恶性直肠息肉的定义是侵犯粘膜肌层直达粘膜下层(pT1)。息肉定义为原位癌时则未穿透至粘膜下层,不会出现区域淋巴结转移。委员会推荐结肠镜检时对癌性息肉进行标记或是如果外科医生认为有必要 2 周内再手术。对有蒂或无蒂息肉(腺瘤),如果息肉已完全切除且组织学特征良好则无需进一步手术。组织学特征良好包括 1/2 级病灶且无血管淋巴侵犯、阴性切缘。对完全切除、单个标本、无蒂息肉(pT1)且组织学特征良好、切缘干净的病人,可以考虑观察,但需知道此类息肉的负性结果发生率明显高于多发恶性息肉,负性结果包括残留、复发、死亡率和血行转移而非淋巴结转移。此类病人也可选直肠手术。直肠手术也推荐用于息肉伴有不良组织学特征、标本破坏或边缘不能评价。腺瘤不良组织学特征是 3 或 4 级、血管淋巴侵犯、阳性切除边缘。此种病人淋巴结受累风险增高。目前尚无阳性切缘共识定义,内镜切除息肉的阳性切缘指的是距横切缘的 1-2mm 内存在肿瘤或是热疗法的横切缘中存在肿瘤细胞。对息肉不完整的标本或边缘不能评价标本,推荐经肛切除或是经腹切除。具有不良组织学特征者,应考虑经腹部切除以包括淋巴结切除。术前内镜超声可能会提供更多信息以指导手术方法选择,虽然这种方法检测肿瘤残留的精确性有限。所有进行了息肉切除的病人应进行随访。2. 治疗局限性直肠癌直肠癌的定义是硬直肠镜检显示癌性病灶位于肛缘 12cm 内。决定直肠癌病人治疗计划很复杂,除了要确定直肠癌手术治疗目的(治愈还是姑息),还必需考虑治疗造成的功能改变。需维持或恢复正常肠功能和肛门功能的可能性以及保留泌尿生殖功能。对远端直肠癌既要达到治愈目的又要对生活质量影响最小,很具有挑战性。直肠癌盆腔复发风险比结肠癌高,局部复发与预后不良相关。进行特别治疗时要仔细选择病人,采用序贯多种模式治疗,对有选择的病人推荐联合放化疗结合手术治疗。(1)临床评估 / 分期对直肠癌病人的初始评估为疾病临床分期提供了重要的围手术期信息。临床分期用于指导治疗选择,包括手术倾向及手术方法,是否推荐围手术期放化疗,临床过分期或分期不足的影响都很大。对起始表现适合手术切除的病人需要彻底分期,包括全结肠镜评估同时发生的病灶或其它病理学情况,硬直肠镜判断癌症位置(如测量肿瘤距肛缘距离)。此外其它检查如 CEA、PS 评分状态以确定手术风险。通过影像学方法评估,如直肠内超声可以术前评估肿瘤穿透深度和是否存在淋巴结转移。关于疾病侵犯程度的更多信息和远处转移的发生可以通过术前 CT 检查明确。内镜超声或盆腔 MRI、胸、腹和盆腔 CT 推荐用于直肠癌的术前分期。CT 应采用静脉和口服增强,如果腹部和盆腔 CT 不充足或增强 CT 不适合,可考虑 MRI 增强检查。委员会共识是 PET 扫描不需常规采用,如果进行了 PET/CT 也不能用其代替增强 CT。PET/CT 应当仅用于评估增强 CT 结论模糊的结果或是病人静脉使用造影剂有禁忌症。有研究分析了内镜超声、MRI 和 CT 用于术前对直肠癌分期的精确性,证实内镜超声和 MRI 评估肿瘤穿透入肌层深度的敏感性相似,内镜超声评估局部肿瘤侵犯的特异性较 MRI 强,目前 CT 用于术前 T 分期并非优选。精确评估淋巴结受累的敏感性和特异性时只有 CT 和 MRI 能评估髂骨、肠系膜和后腹膜淋巴结,也有研究认为 CT、MRI 和超声都不是最好的评价方法。临床分期也依赖活检或局部切除标本的组织学检查,内镜活检标本应仔细的病理评估寻找侵犯粘膜肌层的证据,如果考虑切除直肠,应尽早咨询肠造瘘专家以更好的术前标记位置,并对病人进行教育。(2)评估治疗反应新辅助治疗后要重新分期以计划手术方式,或是某些病人可能不需要手术或其它治疗。MRI、CT 或 EUS 是最常用的重新分期手段,评估 T 分期和淋巴结受累很有效。功能性 MRI 技术可以测定微循环、血管通透性和组织细胞密度,有助于决定新辅助化疗反应重新分期。(3)手术方式术式依赖疾病的位置和程度,主要治疗原发直肠癌病灶。方式包括局部处理如息肉切除、经肛切除和经肛内镜微手术(TEM);侵袭性程序包括经腹切除联合结肠肛吻合术。(4)经肛切除经肛切除只适合选择性的 T1、N0 早期癌症,小于 3cm、中高分化、距肛缘 8cm、小于 30% 的直肠周缘、没有淋巴结受累者,可以经肛切除并保证阴性切缘。如果病灶完全在直肠内,TEM 方便经肛门切除小肿瘤,TEM 从技术角度对更近端的肿瘤具有可行性。经肛切除和 TEM 皆包括垂直肠壁至直肠周围脂肪的全层切除。需要获得阴性深切缘(大于 3mm)和粘膜切缘,避免肿瘤破碎。切除标本应在固定前标记好再行送检以便利病理医生检查。局部治疗的优势是并发症最少、死亡率最低、术后恢复很快。如果病理检查存在不良特征如阳性边缘、淋巴血管浸润、分化差、侵袭粘膜下层的下 1/3,就应行更加根治性切除。经肛切除的局限性包括缺少受累淋巴结病理分期,有证据显示淋巴结微转移在早期直肠病灶很常见而且不可能由直肠内镜超声鉴定出来。这可能解释了局部切除局部复发更高的原因。因此需仔细选择进行局部切除 T1N0 直肠癌,仔细检查切除标本,如果发现 T2 疾病或具有高危特征应行经腹切除。(5)经腹切除不满足局部手术要求的病人应当接受经腹切除。保留括约肌功能的保肛手术是优选治疗方案,但不是所有病例都能达到。术前放化疗可使肿瘤大小下降,使一些初始因肿块较大的肿瘤括约肌保留成为可能。经腹切除手术推荐 TME。TME 包括整体切除直肠系膜,包括相关血管和淋巴结结构、脂肪组织及直肠系膜筋膜,方法是通过锐性分离并保留自主神经。淋巴引流区受直肠肿瘤位置影响,更多的远端肿瘤向上和侧方淋巴引流,近端肿瘤更多只向上引流。TME 方法能根治性移除上方肿瘤的淋巴回流区域,委员会不推荐扩大淋巴结切除,除非这些淋巴结临床看起来可疑受累。如果肛门功能保留且远端清扫干净则 TME 后再行结肠肛吻合术。对中上段直肠,TME 的 LAR 可延伸至肿瘤远端下缘下的 4-5cm 再行结直肠吻合,这是一种治疗选择。如果不能吻合则需行结肠造瘘。较宽的 TME 便于充分的淋巴结切除增加阴性环周切缘可能。如果肿瘤直接侵入肛门括约肌或是肌提肌则需行 APR 和 TME 联合治疗。如果手术必然会导致肛门括约肌功能丧失出现便失禁,APR 对于肿瘤切除边缘阴性是必要的。APR 包括整块移除直肠乙状结肠、直肠和肛门周边的肠系膜、直肠系膜和肛周软组织,此种程序必然需要结肠瘘口。TME 后的手术标本评估很重要,包括大体评估外观、完整性及 CRM。委员会定义当肿瘤在切缘 1mm 内时为阳性 CRM。直肠系膜标本质量的评估可以参照 Dutch Rectal Cancer Trial 中的评分进行。(6)腹腔镜切除关于腹腔镜治疗直肠癌的研究数据较少。就目前而言,腹腔镜手术治疗直肠癌更适合临床试验。(7)可切除非转移性疾病的辅助和新辅助治疗II 期或 III 期直肠癌的新辅助和辅助治疗包括区域性治疗,因其局部复发风险高,风险因素包括与盆壁结构和器官位置较近、缺少浆膜包绕、技术上难以获得更宽的手术切缘。而结肠癌的辅助治疗更强调预防远处转移,因为结肠癌的特征是局部复发风险较低。虽然放疗能减少直肠癌的局部复发率,但也增加毒性。对于一些复发风险低的病人可能手术和辅助化疗就足矣,这样的病人为近端 T3N0M0 直肠癌。但临床中常存在分期不足,因此指南推荐病人仍应前术前放化疗。联合治疗模式中包括手术、联合放化疗、化疗,推荐用于 II 或 III 期直肠癌病人。围手术期盆腔 RT 指南推荐二个治疗顺序,一是术前放化疗,术后化疗;二是化疗、放化疗后手术。围手术期治疗时间,包括化疗和放化疗在内不应超过 6 个月。①对于术前还是术后放疗,委员会推荐术前对 II 或 III 期病人进行放化疗。术后放化疗推荐用于 I 期直肠癌病理评估后分期上调者。术后放化疗方案通常为三明治疗法,化疗用于联合放化疗之前和之后,方案典型为含有 5-FU 的化疗方案。②对于联合放化疗的可能优势包括局部放疗增敏、全身控制疾病、术前放化疗增加保留肛括约肌和病理完全反应的可能。放化疗中主要使用的化疗药物是 5-FU。委员会推荐卡培他滨可替代 5-FU,不推荐奥沙利铂用于新辅助放化疗,不推荐贝伐单抗、西妥昔单抗、帕尼单抗、伊立替康用于联合放化疗。③诱导化疗的可能优势包括早期预防和去除微转移灶,更高的病理学反应率,将回肠造口术时间缩至最小,便于切除,改善耐受性,提高完成化疗的比率。因此诱导化疗在 2015 版作为可接受的选择。④对于术前只行新辅助化疗不行新辅助放化疗可能会减少放疗的毒性作用。⑤多个放射野要包括肿瘤、瘤床及周围 2-5cm 边缘、骶前及髂内淋巴结,对 T4 肿瘤侵犯前部结构者还要包括髂外淋巴结,肿瘤侵入远端肛管者要考虑包括腹股沟淋巴结。推荐剂量 45-50Gy,25-28 次完成。鼓励使用减少小肠放疗剂量的技术和定位,调强放疗(IMRT)仅用于临床试验或复发疾病的再放疗。术前治疗、手术及辅助化疗合作很重要。术前放化疗病人,委员会推荐完成全量放化疗后间隔 5-12 周再行手术,以利恢复。虽然更长间隔可能增加病理完全缓解率,但不清楚是否有临床获益。如果临床需要更长间隔,也不会导致失血、手术耗时及阳性边缘率增加。⑥短程放疗与传统放疗相比局部控制与 OS 都相同,可作为一种治疗选择。⑦新辅助治疗的反应与长期结果、远处转移、局部复发等相关。新辅助治疗后肿瘤降期至 yT1-2 者更易从术后辅助治疗中获益,对这类病人更应进行辅助治疗。⑧对新辅助治疗获得完全缓解者委员会不支持等待观望的方法处理。⑨所有 II 或 III 期直肠癌病人在完成新辅助放化疗和手术治疗后,如果没有接受术前新辅助化疗者,都要接受辅助化疗。委员会推荐 FOLFOX 或 CapeOX 方案优选,FLOX、5-FU/LV 卡培他滨也可应用。(8)T1 或 T2 病人的治疗推荐淋巴结阴性 T1 病灶可经腹切除或是经肛切除。若局部切除病理评估显示分化差、阳性边缘、侵袭入粘膜下层的下 1/3、淋巴血管侵犯或再分期 T2,应重新经腹切除。对高危病人又不能接受再手术者需行三明治模式的化疗、放化疗、化疗进行治疗,以减少治疗不足,因为这种病人的淋巴结状态未知。淋巴结阴性 T2 病灶应接受经腹切除,因单纯局部切除局部复发率可达 11%-45%。经腹切除后 pT1-2,N0,M0 者不需继续治疗,若 pT3,N0,M0 或淋巴结阳性,需行三明治模式治疗,包括一周期辅助化疗,采用 5-FU/LV、FOLFOX 或卡培他滨±奥沙利铂,然后 5-FU/RT 或卡培他滨 /RT,最后 5-FU/LV、FOLFOX 或卡培他滨±奥沙利铂。委员会推荐围手术期治疗总的持续时间大约 6 个月。病理证据为 pT3,N0,M0 且切缘阴性、预后特征良好者应一线切除治疗,RT 获益可能较小,单独化疗应考虑。(9)T3 或 T4、淋巴结受累、局部不可切除或病人不能耐受切除的治疗推荐病人为 T3-4,N0 或任何 T,N1-2 或局部不可切除或不能耐受手术者的治疗顺序有二种选择,一是化放疗,然后若可切除就行切除,再行化疗;二是化疗,然后放化疗,然后若可切除就行切除。5-FU/RT 或卡培他滨 /RT 是优选方案;优选化疗方案 FOLFOX 或 CapeOX;切除前应考虑术前治疗,除非存在楚忌症。委员会建议治疗反应差不是不可切除的必然结果,手术探查是恰当的。经腹切除应在新辅助治疗结束后 5-12 周进行,围手术期治疗共约 6 个月;若初始治疗后手术不适合,应全身治疗,此时 FOLFOXIRI 可接受。T3,N0 或任何 T,N1-2 手术可一线治疗,适合不宜放化疗的病人。经腹切除后病理分期 p T1-2,N0,M0 则仅需观察;病理分期 p T3,N0,M0 或 p T1-3,N1-2,M0 接受大约 6 个月的三明治方案治疗;病理近端 T3,N0,M0 且边缘阴性、预后特征良好者经腹手术切除后 RT 获益较小,可考虑单纯化疗。对不能切除的肿瘤,放疗剂量应高于 54Gy,小肠的放射剂量应限于 45Gy。对 T4 肿瘤或复发癌症或边缘很近或阳性者,术中 RT(IORT)利于切除,它是将肿瘤在术中直接暴露于 RT。如果 IORT 不能执行,10-20Gy 或近距离照射则应考虑。八.转移性疾病的治疗原则参见 NCCN 结肠癌指南(2015.2 最新版)九.治疗局部复发疾病局部复发的直肠癌特征是盆腔或吻合口复发。潜在可切除的孤立的盆腔或吻合口复发通常为切除治疗,然后予以辅助性放化疗或围手术期放疗和联合 5-FU 输注。IORT 或近距离照射应在切除时考虑应用。IMRT 可用于再照射的病人。不可切除的病灶给予化疗,放疗根据病人耐受能力酌情加减。去块治疗不推荐。十.治疗后监测参见 NCCN 结肠癌指南(2015.2 最新版)十一.总结NCCN 委员会认为多学科协作治疗直肠癌非常重要;充分病理评估,若可能至少要评估 12 个淋巴结;早期病人且内镜超声或 MRI 证实淋巴结阴性、满足标准者可选用经肛切除;经腹切除适用于其余直肠癌;围手术期放化疗和化疗对大部分怀疑或证实为 T3-4 的病人或有区域淋巴结受累病人是优选治疗策略。推荐的术后监测程序包括 CEA,胸、腹和盆腔 CT 及结肠镜。局部复发者应考虑切除,并接受化疗和放疗。如果不能切除则行化疗,放疗可酌情。有肺、肝转移病人如果可完全切除应考虑手术切除。围手术期化疗和放化疗用于同时转移,围手术期化疗用于非同时转移。病人具有弥漫不可切除转移性疾病者推荐进行连续的治疗。启动治疗时要考虑的原则包括预先计划好的改变治疗时的策略。初始治疗选择要考虑病人是否能耐受强治疗,较强的初始治疗包括 FOLFOX、FOLFIRI、CapeOX 和 FOLFOXIRI,也可加入生物制剂。委员会支持病人优先进入临床试验。
吴庆华 副主任医师 上海瑞金医院 普外科2536人已读





